Đánh giá lâm sàng và miễn dịch đối với nhiễm SARS-CoV-2 không triệu chứng
Đánh giá:
Các đặc điểm lâm sàng và đáp ứng miễn dịch của những người không có triệu chứng bị nhiễm hội chứng hô hấp cấp tính nặng coronavirus 2 (SARS-CoV-2) chưa được mô tả rõ. Chúng tôi đã nghiên cứu 37 cá nhân không có triệu chứng ở quận Vạn Châu được chẩn đoán nhiễm SARS-CoV-2 được xác nhận bằng PCR RT nhưng không có bất kỳ triệu chứng lâm sàng liên quan nào trong 14 ngày trước đó và trong khi nhập viện. Các cá nhân không có triệu chứng đã được đưa vào Bệnh viện Nhân dân Wan Châu do chính phủ chỉ định để cách ly tập trung theo chính sách1. Thời gian trung bình của sự phát tán virus trong nhóm không có triệu chứng là 19 ngày (phạm vi liên vùng (IQR), 15 phản 26 d). Nhóm không có triệu chứng có thời gian phát tán virus lâu hơn đáng kể so với nhóm có triệu chứng (log-rank P = 0,028). Nồng độ IgG đặc hiệu của virut trong nhóm không có triệu chứng (trung bình S / CO, 3,4; IQR, 1,6 cạn10,7) thấp hơn đáng kể (P = 0,005) so với nhóm có triệu chứng (S / CO trung bình, 20,5; IQR, 5,8 ) trong giai đoạn cấp tính. Trong số những người không có triệu chứng, 93,3% (28/30) và 81,1% (30/37) đã giảm nồng độ kháng thể IgG và trung hòa, trong giai đoạn điều trị sớm, so với 96,8% (30,31) và 62,2% ( 23/37) của bệnh nhân có triệu chứng. Bốn mươi phần trăm các cá nhân không có triệu chứng trở nên huyết thanh và 12,9% nhóm triệu chứng trở nên âm tính với IgG trong giai đoạn nghỉ dưỡng sớm. Ngoài ra, các cá nhân không có triệu chứng biểu hiện mức độ thấp hơn của 18 cytokine pro và chống viêm. Những dữ liệu này cho thấy những người không có triệu chứng có đáp ứng miễn dịch yếu hơn với nhiễm SARS-CoV-2. Việc giảm nồng độ IgG và trung hòa kháng thể trong giai đoạn nghỉ dưỡng sớm có thể có ý nghĩa đối với chiến lược miễn dịch và khảo sát huyết thanh học.
Điểm chính:
Kể từ ngày 24 tháng 5 năm 2020, đại dịch bệnh coronavirus 2019 (COVID-19), do SARS-CoV-2 gây ra, đã ảnh hưởng đến hơn 5 triệu người trên thế giới. Hầu hết bệnh nhân bị nhiễm SARS-CoV-2 được báo cáo mắc bệnh hô hấp từ nhẹ đến nặng với các triệu chứng như sốt, ho và khó thở, có thể xuất hiện 2 Hồi14 sau khi tiếp xúc. Tuy nhiên, có những bệnh nhân khác được chẩn đoán bằng xét nghiệm PCR RT dương tính nhưng không có triệu chứng hoặc không có triệu chứng tối thiểu2,3,4,5,6. Bằng chứng ngày càng tăng cho thấy các cá nhân không có triệu chứng có thể lây lan vi-rút một cách hiệu quả và sự xuất hiện của những người truyền bệnh thầm lặng này của SARS-CoV-2 đã gây ra những khó khăn trong việc kiểm soát dịch bệnh 2,5. Tuy nhiên, hiểu biết của chúng tôi về các đặc điểm lâm sàng và đáp ứng miễn dịch của những người không có triệu chứng với nhiễm SARS-CoV-2 còn hạn chế. Ở đây chúng tôi mô tả các đặc điểm dịch tễ và lâm sàng, mức độ vi rút và đáp ứng miễn dịch ở 37 cá nhân không có triệu chứng.
Kết quả:
Đặc điểm dân sốVào ngày 6 tháng 2 năm 2020, Ủy ban Y tế Quốc gia Trung Quốc đã cập nhật Kế hoạch phòng ngừa và kiểm soát COVID-19 (ấn bản thứ 4) để quản lý các liên hệ chặt chẽ, nhấn mạnh việc xác định và cách ly các cá nhân không có triệu chứng1. Để xác định các cá nhân không có triệu chứng, Trung tâm kiểm soát và phòng ngừa dịch bệnh (CDC) của quận Wan Châu sau đó đã tiến hành sàng lọc PCR RT PCR mở rộng cho 2.088 người tiếp xúc gần gũi khi được kiểm dịch. Các cá nhân có kết quả PCR RT dương tính sau đó được sàng lọc bằng các khảo sát về tỷ lệ lưu hành điểm được thực hiện bởi CDC địa phương và các đánh giá triệu chứng được báo cáo bởi các bác sĩ lâm sàng. Trong số này, 60 cá nhân tuyên bố không có triệu chứng nào trong 14 ngày trước đó, theo hồ sơ CDC địa phương, và đã được chuyển đến một bệnh viện do chính phủ chỉ định để cách ly tập trung. Khi nhập viện, 17 cá nhân đã được loại trừ các triệu chứng nhẹ hoặc không điển hình dựa trên các đánh giá triệu chứng được báo cáo bởi các bác sĩ lâm sàng; sáu cá nhân phát triển triệu chứng 41717 sau khi nhập viện cũng bị loại trừ. Cuối cùng, 37 trường hợp không có triệu chứng, được xác định là những cá nhân có kết quả xét nghiệm axit nucleic dương tính nhưng không có bất kỳ triệu chứng lâm sàng liên quan nào trong 14 ngày trước đó và trong khi nhập viện, đã được đưa vào nghiên cứu này. Tổng cộng có 178 bệnh nhân bị nhiễm SARS-CoV-2 được xác nhận đã được xác định tại quận Vạn Châu trước ngày 10 tháng 4 năm 2020, theo dõi bởi các hệ thống giám sát CDC. Trong nghiên cứu này, tỷ lệ bệnh nhân bị nhiễm trùng không triệu chứng là 20,8% (37/178).Để phát hiện kháng thể và đo cytokine, 37 bệnh nhân có triệu chứng nhẹ phù hợp với giới tính, tần số tuổi và độ hấp thụ đã được chọn để so sánh với các cá nhân không có triệu chứng (Bảng bổ sung 1). Ba mươi bảy cá nhân đối chứng phù hợp với giới tính và tần số phù hợp với giới tính từ Quận Vạn Châu với kết quả PCR RT âm tính với SARS-CoV-2 cũng được chọn để so sánh với cytokine.Trong số 37 cá nhân không có triệu chứng, tuổi trung bình là 41 tuổi (tầm 8 tuổi75) và 22 người là nữ. Hai mươi tám cá nhân có tiền sử tiếp xúc với bệnh nhân được xác nhận PCR RT với COVID-19, và chín người là cư dân Vũ Hán hoặc có tiền sử du lịch đến Vũ Hán trước khi bắt đầu nhiễm trùng (Bảng bổ sung 2). Kết quả xét nghiệm phóng xạ và xét nghiệmCông thức máu toàn phần, sinh hóa máu, chức năng đông máu, chức năng gan và thận và dấu ấn sinh học nhiễm trùng được đo khi nhập viện (Bảng bổ sung 2) để theo dõi tiến triển bệnh tiềm ẩn, theo Hướng dẫn điều trị COVID-19 (ấn bản 5) Ủy ban Trung Quốc7. Trong số 37 cá nhân không có triệu chứng, ba người bị giảm bạch cầu và một người bị giảm tiểu cầu. Sáu cá nhân có nồng độ alanine aminotransferase tăng cao và 11 người có mức protein phản ứng C tăng. Khi nhập viện, chụp cắt lớp vi tính ngực (CT) cho thấy các hình mờ thủy tinh mặt đất ở 11 cá thể không có triệu chứng (11/37, 29,7%) và bóng sọc và / hoặc củng cố khuếch tán ở mười cá nhân (10/37, 27,0%), trong khi 16 các cá nhân (16/37, 43,2%) không có bất thường (Hình 1). Năm cá nhân đã phát triển các thuốc mờ thủy tinh mặt đất tiêu cự hoặc bóng sọc trên CT ngực trong vòng 5 ngày sau khi nhập viện. Không có tràn dịch màng phổi, dấu hiệu phế quản không khí hoặc các hạch bạch huyết mở rộng, đó là những thay đổi điển hình được thấy ở bệnh nhân có triệu chứng nghiêm trọng8,9,10. Kết quả X quang bất thường giới hạn ở một phổi được xác định ở 66,7% (14/21) ở những người không có triệu chứng, trong khi 33,3% (7/21) có bất thường ở cả hai phổi.

Hình 1: CT ngực quét từ hai bệnh nhân không có triệu chứng.
a, CT scan của một phụ nữ 45 tuổi cho thấy các mảnh thủy tinh mặt đất khu trú ở thùy dưới của phổi trái (mũi tên). b, CT scan của một phụ nữ 50 tuổi cho thấy các mảnh và sọc thủy tinh mặt đất cùng tồn tại ở thùy dưới của phổi phải (mũi tên).
Kết quả virus học
Chúng tôi đã so sánh các giá trị ngưỡng chu kỳ RT PCR PCR (CT) của gạc mũi họng dương tính đầu tiên cho tất cả 37 cá nhân không có triệu chứng và 37 bệnh nhân có triệu chứng. Các giá trị Ct ban đầu cho 37 cá nhân không có triệu chứng và 37 bệnh nhân có triệu chứng xuất hiện tương tự (ORF1b 32.8 (IQR, 30.9 .35.8) so với 31.7 (IQR, 30.3. IQR, 31.3 Ném37.2), P = 0.126) (Hình 2a). Thời gian trung bình của sự phát tán virus, được định nghĩa là khoảng thời gian từ tăm bông mũi họng dương tính đầu tiên và cuối cùng, ở những người không có triệu chứng là 19 ngày (IQR, 15 Ném26 d). Thời gian quan sát ngắn nhất của sự phát tán virus là 6 ngày, trong khi thời gian dài nhất là 45 ngày. Thời gian trung bình của sự phát tán virus là 14 ngày (IQR, 9 trận22 d) ở những bệnh nhân có triệu chứng nhẹ. Nhóm không có triệu chứng có thời gian phát tán virus lâu hơn đáng kể so với nhóm có triệu chứng (log-rank P = 0,028) (Hình 2b). Tuy nhiên, sự phát tán virus có thể đo được không tương đương với sự lây nhiễm của virus và cần đánh giá thêm để xác định tải lượng virus SARS-CoV-2 hô hấp có tương quan với virus có thể nuôi cấy11.
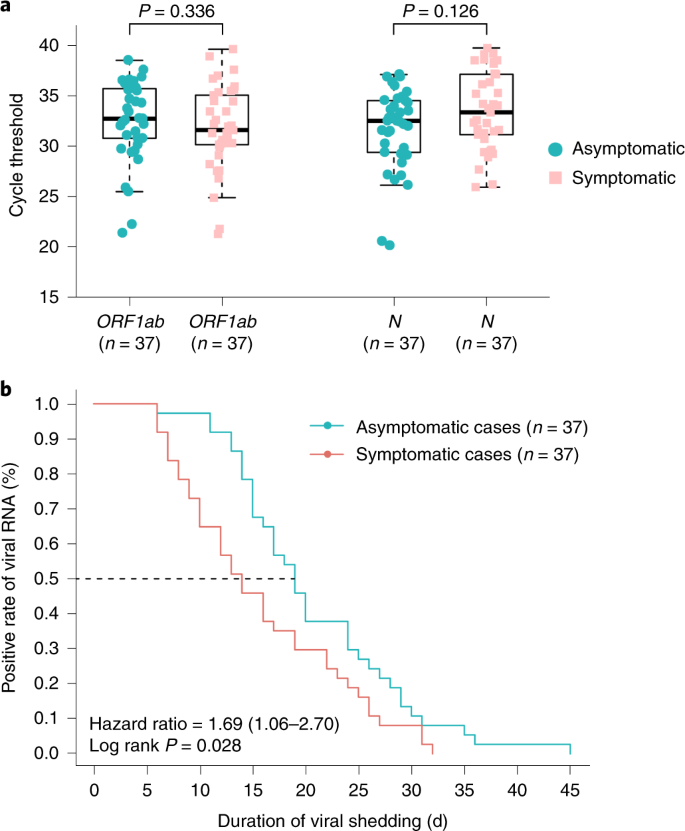
Hình 2: Đặc điểm virus học trong các trường hợp không có triệu chứng và triệu chứng.
a, Các giá trị Ct của ORF1b và N thu được bằng RT PCR PCR được phát hiện trong bệnh phẩm mũi họng từ các nhóm không triệu chứng (n = 37) và triệu chứng (n = 37). Các ô hình hộp cho thấy các dải phân cách (đường giữa) và các tứ phân vị thứ nhất và thứ ba (các hộp), trong khi các ô râu hiển thị 1,5 × IQR ở trên và dưới hộp. Không ghép đôi, các giá trị P thử nghiệm MannTHER Whitney U hai mặt được mô tả trong các ô và mức cắt giá trị P đáng kể được đặt ở 0,05. b, Phương pháp Kaplan Vi Meier được sử dụng để ước tính tỷ lệ RNA dương tính và xét nghiệm xếp hạng log hai mặt được áp dụng để đánh giá sự khác biệt có ý nghĩa của thời gian phát tán virus trong các nhóm có triệu chứng và không có triệu chứng.
IgG và IgM đặc hiệu với virut ở người không có triệu chứng
Để điều tra phản ứng kháng thể cấp tính với nhiễm SARS-CoV-2, IgG và IgM đặc hiệu của virus được đo trong các mẫu huyết thanh từ các cá nhân không có triệu chứng và không có triệu chứng. Trong nhóm không có triệu chứng, 81,1% (30/37) cho kết quả dương tính với IgG và 83,8% (31/37) của nhóm có triệu chứng được xét nghiệm dương tính với IgG khoảng 3 tuần4 sau khi tiếp xúc. Hơn nữa, 62,2% (23/37) của nhóm không có triệu chứng dương tính với IgM, trong khi 78,4% (29/37) của nhóm có triệu chứng là IgM dương tính. Điều thú vị là nồng độ IgG trong nhóm triệu chứng (S / CO trung bình, 20,5; IQR, 5,8 giai đoạn mà RNA virus có thể được tìm thấy trong một mẫu vật hô hấp) (P = 0,005) (Hình 3a).
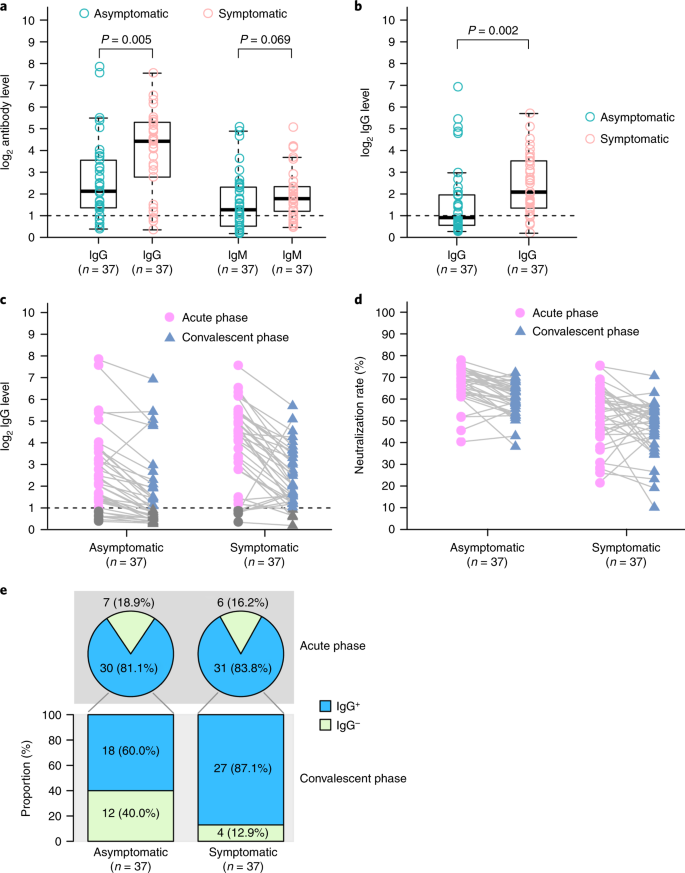
Hình 3: Nồng độ IgG và IgM trong giai đoạn cấp tính và nghỉ dưỡng ở bệnh nhân nhiễm SARS-CoV-2.
a, So sánh nồng độ kháng thể đặc hiệu của virus ở bệnh nhân không có triệu chứng (n = 37) và bệnh nhân có triệu chứng (n = 37) với nhiễm trùng cấp tính. b, Nồng độ IgG ở bệnh nhân COVID-19 giai đoạn nghỉ dưỡng được xuất viện. c, Thay đổi năng động về mức độ IgG đặc hiệu của virus trong các giai đoạn cấp tính và nghỉ dưỡng. d, Những thay đổi năng động trong việc trung hòa các kháng thể trong huyết thanh trong các giai đoạn cấp tính và nghỉ dưỡng. Kết quả được biểu thị bằng trung bình của hai thí nghiệm độc lập. e, tỷ lệ IgG dương tính của bệnh nhân mắc COVID-19 trong giai đoạn cấp tính và nghỉ dưỡng. Các ô trong ô a và b hiển thị trung vị (đường giữa) và tứ phân vị thứ nhất và thứ ba (hộp) và râu ria hiển thị 1,5 × IQR ở trên và dưới hộp. Không ghép đôi, các giá trị P thử nghiệm MannTHER Whitney U hai mặt được mô tả trong các ô và mức cắt giá trị P đáng kể được đặt ở 0,05.
Chúng tôi cũng theo dõi 37 cá nhân không có triệu chứng và 37 bệnh nhân có triệu chứng vào giai đoạn nghỉ dưỡng sớm (8 tuần sau khi họ được xuất viện). Nồng độ IgG trong nhóm triệu chứng vẫn cao hơn đáng kể so với nhóm không có triệu chứng ở giai đoạn nghỉ dưỡng sớm (P = 0,002) (Hình 3b). Đáng ngạc nhiên, nồng độ IgG trong 93,3% (28/30) của nhóm không có triệu chứng và 96,8% (30,31) của nhóm triệu chứng đã giảm trong giai đoạn nghỉ dưỡng sớm (Hình 3c). Tỷ lệ phần trăm giảm trung bình là 71,1% (phạm vi, 32,8 .88,8%) đối với các mức IgG trong nhóm không có triệu chứng, trong khi tỷ lệ giảm trung bình là 76,2% (phạm vi, 10,9 mật96,2%) trong nhóm triệu chứng. Sử dụng xét nghiệm trung hòa dựa trên pseudovirus (Phương pháp), chúng tôi cũng quan sát thấy sự giảm nồng độ kháng thể trong huyết thanh ở 81,1% (30/37) của nhóm không có triệu chứng và ở 62,2% (23/37) của nhóm triệu chứng. Tỷ lệ phần trăm giảm trung bình là 8,3% (phạm vi 0,5 0,522,8%) để trung hòa các kháng thể trong huyết thanh ở nhóm không có triệu chứng, trong khi tỷ lệ giảm trung bình là 11,7% (phạm vi, 2,3 Nott41,1%) trong nhóm triệu chứng (Hình 3d ). Hơn nữa, 40,0% (12/30) của các cá nhân không có triệu chứng, nhưng chỉ có 12,9% (4/31) các cá nhân có triệu chứng, đã trở thành huyết thanh đối với IgG (Hình 3e).
Cytokine ở những người không có triệu chứng
Để làm rõ hơn các phản ứng miễn dịch liên quan đến nhiễm SARS-CoV-2, nồng độ cytokine và chemokine huyết thanh được so sánh giữa các nhóm không có triệu chứng và triệu chứng. Nồng độ tăng cao của 18 cytokine pro và chống viêm đã được quan sát trong nhóm triệu chứng so với nhóm không có triệu chứng. Trong số này, phối tử gây ra apoptosis liên quan đến yếu tố hoại tử khối u (TRAIL) (P = 3,39 × 10−14), yếu tố kích thích đại thực bào (M-CSF) (P = 5.08 × 10−13), oncogene điều hòa tăng trưởng α (GRO-α) (P = 1,5 × 10−10), yếu tố kích thích khuẩn lạc bạch cầu hạt (G-CSF) (P = 2.05 × 10−9) và interleukin 6 (IL-6) (P = 6,33 × 10− 9) cho thấy những thay đổi quan trọng nhất (Hình 4 và Dữ liệu mở rộng Hình 1). Hơn nữa, các cytokine đã được phân tích sâu hơn trong nhóm không có triệu chứng và 37 nhóm đối chứng khỏe mạnh. Nồng độ 32 cytokine trong huyết tương tương tự nhau giữa nhóm đối chứng khỏe mạnh và người không có triệu chứng. Mức độ cao hơn đáng kể của yếu tố tế bào gốc (SCF) (P = 1,48 × 10−9), IL-13 (P = 3,75 × 10−7), IL-12 p40 (P = 7,08 × 10−6) và yếu tố ức chế bệnh bạch cầu (LIF) (P = 1.33 × 10−3) đã được tìm thấy trong nhóm không có triệu chứng (Dữ liệu mở rộng Hình 2). Tổng hợp, dữ liệu của chúng tôi cho thấy các cá nhân không có triệu chứng có phản ứng viêm giảm đặc trưng bởi nồng độ cytokine và chemokine lưu hành thấp.
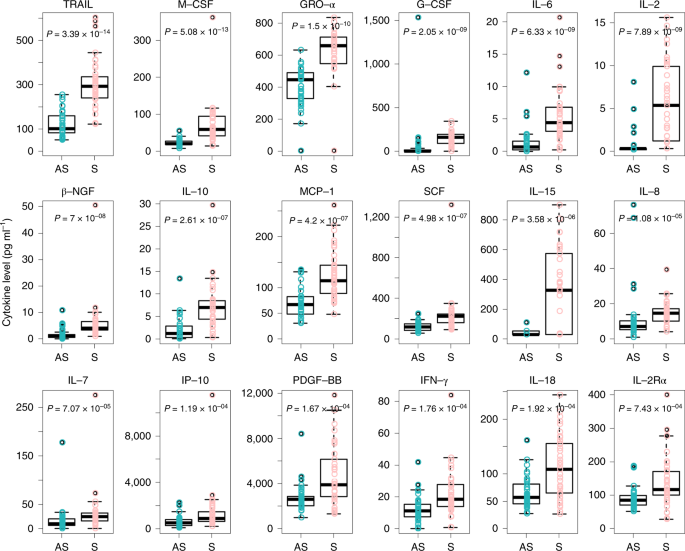
Hình 4: So sánh nồng độ cytokine / chemokine trong huyết thanh giữa các nhóm không có triệu chứng và triệu chứng.
Các mẫu từ bệnh nhân không có triệu chứng (n = 37) và triệu chứng (n = 37) với COVID-19 được thu thập trong giai đoạn cấp tính khi nhập viện, và các xét nghiệm đã được thực hiện để đo nồng độ 48 cytokine và chemokine. Các ô hình hộp cho thấy các dải phân cách (đường giữa) và các tứ phân vị thứ nhất và thứ ba (các hộp) và râu ria hiển thị 1,5 × IQR ở trên và dưới hộp. Không ghép đôi, các giá trị P thử nghiệm MannTHER Whitney U hai mặt được mô tả trong các ô và mức cắt giá trị P đáng kể được đặt ở mức 0,001.
Thảo luận
Các đặc điểm lâm sàng và đáp ứng miễn dịch của những người không có triệu chứng bị nhiễm SARS-CoV-2 chưa được mô tả rõ. Trong số 178 bệnh nhân được xác nhận trong phòng thí nghiệm, 37 người không bao giờ phát triển bất kỳ triệu chứng nào trong suốt quá trình điều trị bệnh được đưa vào nghiên cứu này. Dữ liệu của chúng tôi cho thấy 20,8% bệnh nhân này bị nhiễm trùng không triệu chứng. Tuy nhiên, đây có thể không phải là ước tính chính xác về tỷ lệ nhiễm trùng không triệu chứng trong dân số do thực tế là nhiễm trùng không triệu chứng được xác định từ những người có nguy cơ nhiễm trùng cao (bao gồm cả những người tiếp xúc gần gũi và cá nhân có tiền sử du lịch đến Vũ Hán ) và không phải từ một mẫu người ngẫu nhiên. Do đó, tỷ lệ nhiễm trùng không triệu chứng cần được xác định thông qua sàng lọc dân số12. Ngoài ra, tỷ lệ nhiễm trùng không triệu chứng có thể còn cao hơn vì một số trường hợp có thể bị bỏ qua khi xét nghiệm RT PCR PCR. Nhóm của chúng tôi đã xác định thành công bảy bệnh nhân bị nhiễm SARS-CoV-2 từ 148 trường hợp có kết quả PCR RT âm tính và không có triệu chứng bằng cách sử dụng xét nghiệm kháng thể13. Do đó, nên sử dụng kết hợp xét nghiệm RT và PCR huyết thanh kịp thời, điều này sẽ có lợi cho việc ước tính chính xác tỷ lệ không có triệu chứng. Tuy nhiên, xét nghiệm huyết thanh học có những hạn chế và các xét nghiệm khác nhau về độ đặc hiệu và độ nhạy của chúng. Kết quả cũng có thể bị nhầm lẫn bởi các kháng thể hiện có trước đây với SARS-CoV, MERS-CoV hoặc coronavirus lạnh thông thường.
Cho đến nay, thời gian rụng RNA SARS-CoV-2 vẫn chưa được mô tả rõ ràng. Trong SARS-CoV, RNA virus được phát hiện trong các mẫu bệnh phẩm khác nhau, bao gồm tăm bông, phân và nước tiểu, trong hơn 30% bệnh nhân trong 4 tuần sau khi bệnh khởi phát14. Trong nhiễm trùng MERS-CoV, sự phát tán virus trong dịch tiết đường hô hấp tồn tại ít nhất 3 tuần15. Gần đây, một nghiên cứu trên 191 bệnh nhân mắc COVID-19 đã báo cáo rằng thời gian trung bình của sự phát tán virus là 20 ngày ở những người sống sót (khoảng 8 83737 d) 16. Trong một báo cáo khác, thời gian phát tán virus ở các nguyện vọng mũi họng đã kéo dài đến ít nhất 24 ngày sau khi khởi phát triệu chứng ở 18 bệnh nhân nhiễm SARS-CoV-2 ở Singapore17. Trong nghiên cứu này, thời gian trung bình của sự phát tán virus ở 37 bệnh nhân có triệu chứng nhẹ là 14 ngày, ngắn hơn so với các báo cáo trước đây. So với các bệnh nhân có triệu chứng, nhóm không có triệu chứng có thời gian phát tán virus lâu hơn đáng kể, với thời gian phát tán virus là 19 ngày. Một số yếu tố có thể góp phần vào sự thay đổi thời gian rụng của virus trong các nghiên cứu khác nhau, bao gồm mức độ nghiêm trọng của bệnh, định nghĩa về thời gian rụng của virus và tần suất thu thập mẫu bệnh phẩm. Đáng chú ý, việc phát hiện RNA virus không nhất thiết có nghĩa là virus truyền nhiễm có trong bệnh phẩm hô hấp và cần thận trọng khi áp dụng thời gian phát tán virus được tính toán dựa trên RT PCR PCR để đánh giá khả năng lây nhiễm.
Sức mạnh và thời gian miễn dịch sau khi nhiễm bệnh là những vấn đề chính đối với ‘lá chắn miễn dịch 18 và để thông báo các quyết định về cách thức và thời điểm để giảm bớt các hạn chế khoảng cách vật lý19,20. Các nghiên cứu trước đây đã chỉ ra rằng các kháng thể lưu hành chống lại SARS-CoV hoặc MERS-CoV tồn tại ít nhất 1 năm21,22. Nồng độ IgG duy trì được duy trì trong hơn 2 năm sau khi nhiễm SARS-CoV23,24. Phản ứng kháng thể ở những người bị nhiễm MERS-CoV được xác nhận trong phòng thí nghiệm kéo dài ít nhất 34 tháng sau khi dịch 25. Gần đây, một số nghiên cứu mô tả các phản ứng miễn dịch thích nghi với nhiễm SARS-CoV-2 đã báo cáo rằng hầu hết các cá thể nghỉ dưỡng COVID-19 đều có các kháng thể trung hòa có thể phát hiện được, tương quan với số lượng tế bào T đặc hiệu của virus 26,27,28,29. Trong nghiên cứu này, chúng tôi đã quan sát thấy rằng nồng độ IgG và kháng thể trung hòa ở một tỷ lệ cao những người đã hồi phục sau khi nhiễm SARS-CoV-2 bắt đầu giảm trong vòng 2 Tháng 3 sau khi nhiễm bệnh. Trong một phân tích khác về động lực của việc chuẩn độ kháng thể trung hòa ở tám bệnh nhân điều trị bằng COVID-19, bốn bệnh nhân cho thấy các kháng thể trung hòa giảm khoảng 6 tuần7 sau khi khởi phát bệnh30. Một mô hình toán học cũng cho thấy thời gian miễn dịch ngắn sau khi nhiễm SARS-CoV-231. Cùng với nhau, những dữ liệu này có thể chỉ ra các rủi ro khi sử dụng hộ chiếu miễn dịch COVID-19, và hỗ trợ kéo dài các can thiệp y tế công cộng, bao gồm xa cách xã hội, vệ sinh, cách ly các nhóm có nguy cơ cao và xét nghiệm rộng rãi. Các nghiên cứu huyết thanh học theo chiều dọc bổ sung cho các cá nhân có triệu chứng và không có triệu chứng hơn là cần thiết để xác định thời gian miễn dịch qua trung gian kháng thể. Ngoài ra, nồng độ IgG kháng virut thấp ở bệnh nhân không có triệu chứng, những người có khả năng trở thành huyết thanh cao hơn, hỗ trợ thêm cho nhu cầu sử dụng huyết thanh kịp thời để nghiên cứu tỷ lệ nhiễm trùng thực sự.
Phương pháp
Thiết kế nghiên cứu và người tham gia
Từ ngày 21 tháng 1 đến ngày 19 tháng 2 năm 2020, 25 bệnh nhân có triệu chứng nhập khẩu (đã đăng ký tại huyện Vạn Châu), trở về từ thành phố Vũ Hán hoặc tỉnh Hồ Bắc, đã được xác nhận nhiễm SARS-CoV-2 dựa trên xét nghiệm PCR RT dương tính ở huyện Vạn Châu. (Vạn Châu là khu vực chịu thiệt hại nặng nề nhất của thành phố Trùng Khánh, là một đô thị cấp tỉnh nằm cạnh tỉnh Hồ Bắc.) Tính đến ngày 10 tháng 4 năm 2020, có tổng số 2.088 cá nhân, bao gồm cả những người tiếp xúc gần gũi với bệnh nhân được xác nhận và người trở về từ Vũ Hán, đã được kiểm dịch bởi CDC địa phương và được thử nghiệm bằng RT PCR PCR. Trong số 2.088 cá nhân này, 93 triệu chứng đã phát triển và xét nghiệm dương tính với SARS-CoV-2.
Vào ngày 6 tháng 2 năm 2020, Ủy ban Y tế Quốc gia Trung Quốc đã cập nhật Kế hoạch Kiểm soát và Phòng ngừa COVID-19 (ấn bản thứ 4) để quản lý các liên hệ chặt chẽ, nhấn mạnh việc xác định và cách ly các cá nhân không có triệu chứng. CDC địa phương sau đó đã tiến hành sàng lọc PCR RT RT trên diện rộng cho các cá nhân bị cách ly. Sau khi một trường hợp được xác nhận dương tính với RT PCR PCR, cuộc điều tra tỷ lệ hiện mắc đầu tiên được thực hiện bởi nhân viên CDC địa phương. Các cá nhân được xác nhận có COVID-19 được yêu cầu cung cấp thông tin, bao gồm cả nhân khẩu học (dữ liệu về sinh, giới và bệnh thận), các tình trạng có từ trước (bao gồm tiền sử tăng huyết áp, đái tháo đường, bệnh tim mạch, bệnh mạch máu não, bệnh phổi mãn tính, bệnh thận bệnh gan mạn tính và các bệnh suy giảm miễn dịch) và các triệu chứng, cũng như các hồ sơ sàng lọc trong 14 ngày trước đó (bao gồm sốt, ho, thở ra, khó thở, lạnh, đau cơ, đau họng, chảy nước mũi, đau ngực, tiêu chảy, nôn mửa và nôn buồn nôn). Theo Kế hoạch phòng ngừa và kiểm soát COVID-19 (ấn bản thứ 4), 60 cá nhân không có triệu chứng dựa trên sàng lọc sơ bộ đã được xác định và chuyển đến một bệnh viện do chính phủ chỉ định để cách ly tập trung. Khi nhập viện, các cuộc phỏng vấn trực tiếp được thực hiện bởi các bác sĩ lâm sàng để chứng thực các tuyên bố không có triệu chứng. Sau sàng lọc này, 17 cá nhân đã được loại trừ các triệu chứng nhẹ hoặc không điển hình. Bác sĩ lâm sàng tiến hành sàng lọc triệu chứng hàng ngày một khi một cá nhân được nhập viện. Bốn đến 17 ngày sau khi nhập viện, sáu trong số 43 cá nhân không có triệu chứng trước đây đã phát triển các triệu chứng và được phân loại lại thành triệu chứng. Cuối cùng, 37 cá nhân bị nhiễm trùng không triệu chứng đã được thông báo về nghiên cứu và đồng ý tham gia vào nghiên cứu này.
Không rõ liệu những người có nhiễm trùng không triệu chứng có thể tiến triển thành bệnh lâm sàng trong giai đoạn đầu của dịch SARS-CoV-2 ở Trung Quốc hay không. Do đó, các bác sĩ lâm sàng Trung Quốc đã chọn sử dụng thuốc hít interferon-alpha (IFN-α), điều trị bằng thuốc kháng vi-rút (ribavirin bằng đường uống) và điều trị hỗ trợ (điều trị để tăng cường khả năng miễn dịch, như thymopentin và thuốc Trung Quốc) để tránh làm nặng thêm, theo COVID-19 Hướng dẫn điều trị (ấn bản thứ 5) từ Viện sức khỏe quốc gia Trung Quốc, xuất bản vào ngày 8 tháng 2 năm 2020. Chiến lược cách ly và điều trị nhiễm trùng không triệu chứng nên được cập nhật theo hướng dẫn chính thức ở các quốc gia khác nhau.
Sau đó, 37 bệnh nhân có triệu chứng phù hợp với giới tính, tần số tuổi và độ hấp thụ được chọn để so sánh với các cá nhân không có triệu chứng (Bảng bổ sung 1). Ba mươi bảy điều khiển phù hợp với giới tính và tần số phù hợp với kết quả PCR RT âm tính với SARS-CoV-2 cũng được đưa vào nghiên cứu này. Các cá nhân bị bệnh phổi, gan, thận, tim mạch, chuyển hóa hoặc suy giảm miễn dịch đã được loại trừ.
Thu thập dữ liệu
Dịch tễ học, nhân khẩu học, lịch sử tiếp xúc và tiếp xúc, thuyết trình lâm sàng, CT ngực, xét nghiệm trong phòng thí nghiệm, dữ liệu điều trị và kết quả được thu thập từ hồ sơ y tế nội trú. Dữ liệu phòng thí nghiệm được thu thập cho mỗi bệnh nhân bao gồm công thức máu toàn phần, hồ sơ đông máu, xét nghiệm sinh hóa huyết thanh (bao gồm chức năng thận và gan, điện giải đồ, dehydrogenase và creatine kinase), ferritin huyết thanh và dấu ấn sinh học của nhiễm trùng. Chụp CT ngực đã được thực hiện cho tất cả bệnh nhân nội trú.
Để xác định nhiễm SARS-CoV-2, tăm bông mũi họng được thu thập ít nhất hai lần và được xét nghiệm bằng RT PCR PCR. RNA từ tất cả các mẫu được phân lập trong vòng 24 giờ. Các mẫu RNA virus được chiết xuất theo hướng dẫn của nhà sản xuất bằng cách sử dụng Bộ tách chiết axit Nucleotide (DAAN Gene, đăng ký số 20170583), dựa trên quy trình tinh chế hạt từ tính tự động. Một bộ PCR RT PCR thương mại (DAAN Gene, đăng ký số 20203400063) đã được sử dụng để thử nghiệm các mẫu cho SARS-CoV-2. Tóm lại, hai gen mục tiêu, bao gồm đọc khung frame1ab (ORF1ab) và protein nucleocapsid (N), đồng thời được khuếch đại và thử nghiệm trong RT RT PCR. Các mồi của xét nghiệm RT PCR PCR cho SARS-CoV-2 theo khuyến nghị của CDC Trung Quốc (ORF1ab chuyển tiếp: CCCTGTGGGTTTTACACTTAA, ORF1ab đảo ngược: ACGATTGTGCATCAGCT GA, ORF1ab thăm dò: 5′-CCGGGGGGG chuyển tiếp: GGGGAACTTCTCCTGCTAGAAT, N ngược lại: CAGACATT.
TTGCTCTCAAGCTG, đầu dò N: 5′-TTGCTGCTGCTTGACAGATT-3 (thuốc nhuộm VIC có nhãn)). Chu kỳ PCR: 50 ° C trong 15 phút, 95 ° C trong 15 phút, 45 chu kỳ chứa 94 ° C trong 15 giây, 55 ° C trong 45 giây (thu thập huỳnh quang).
Giá trị Ct nhỏ hơn 37 và lớn hơn 40 được xác định là dương và âm tương ứng cho cả hai gen. Các mẫu có giá trị Ct từ 37 đến 40 được xác định là không kết luận và cần thử nghiệm thứ hai. Bắt đầu 1 tuần sau khi nhập viện, các mẫu mũi họng được xét nghiệm bằng RT PCR PCR cứ sau 2 lần 3 trong 3 thời gian còn lại của thời gian nằm viện. Bệnh nhân có một kết quả PCR RT dương tính được xác định là bệnh nhân nhiễm SARS-CoV-2. Bệnh nhân có hai kết quả PCR RT âm tính liên tiếp được xác định là SARS-CoV-2 âm tính.
Định nghĩa
Một trường hợp được xác nhận của COVID-19 được xác định là một cá nhân có tăm bông mũi họng dương tính với SARS-CoV-2, sử dụng PCR dựa trên phòng thí nghiệm. Các bệnh nhân có triệu chứng được xác định là bệnh nhân có COVID-19 được xác nhận trong phòng thí nghiệm với các triệu chứng như sốt, ho, đau họng và đờm. Một trường hợp không có triệu chứng được xác định là một cá nhân có kết quả xét nghiệm axit nucleic dương tính nhưng không có bất kỳ triệu chứng lâm sàng liên quan nào trong 14 ngày trước đó và trong khi nhập viện. Một tiếp xúc gần gũi được định nghĩa là (1) bất cứ ai ở trong khoảng 6 feet (2 mét) của người bị nhiễm SARS-CoV-2 trong hơn 10 phút và (2) những người tiếp xúc trực tiếp với dịch tiết truyền nhiễm của một bệnh nhân COVID-19. Liên hệ chặt chẽ có thể xảy ra trong khi chăm sóc, sống cùng, thăm hoặc chia sẻ khu vực chờ chăm sóc sức khỏe hoặc phòng với bệnh nhân mắc COVID-19. Thời gian rụng được tính bằng số ngày từ mẫu mũi họng dương tính đầu tiên đến mẫu dương tính cuối cùng dựa trên xét nghiệm RT PCR PCR. Mẫu dương tính cuối cùng được theo dõi bằng kết quả RT PCR PCR âm tính trên hai xét nghiệm liên tiếp.
Phát hiện IgG và IgM chống lại SARS-CoV-2
Theo hướng dẫn của nhà sản xuất, IgG và IgM chống lại SARS-CoV-2 trong các mẫu huyết tương sử dụng bộ xét nghiệm miễn dịch men hóa phát quang từ tính (Bioscience). Tóm lại, các kháng nguyên tái tổ hợp có chứa nucleoprotein và một peptide (LQPELDSFKEELDKYFKNHTSPDVD) từ protein tăng đột biến của SARS-CoV-2 đã bất động trên các hạt từ tính.
Phát hiện trung hòa bằng xét nghiệm trung hòa pseudovirus
Một đột biến được tối ưu hóa bằng mã hóa (S) thiếu 19 axit amin C-terminal 19 đã được sử dụng để tạo ra một pseudovirus biểu hiện luciferase. Xét nghiệm trung hòa pseudovirus SARS-CoV-2 được thực hiện trên các tế bào 293T biểu hiện ACE2 trong một đĩa 96 giếng. Đã thu được huyết thanh pha loãng (1: 600) từ một cá nhân (một mẫu huyết thanh từ pha cấp tính và một mẫu huyết thanh khác từ pha dưỡng bệnh), các thể tích pseudovirus SARS-CoV-2 bằng nhau đã được thêm vào và các đĩa được ủ trước 37 ° C trong 1 giờ. Sau đó, 293T tế bào biểu hiện ACE2 được ủ với 100 μl hỗn hợp sera-pseudovirus trong 24 giờ. Ba ngày sau khi bị nhiễm bệnh, các tế bào được ly giải với 30 μl dung dịch đệm ly giải (Promega) để đo sự tải nạp pseudovirus. Các đơn vị phát quang tương đối của hoạt động luciferase đã được phát hiện bằng cách sử dụng Bộ xét nghiệm Luciferase (Promega), theo hướng dẫn của nhà sản xuất. Các thí nghiệm được lặp lại hai lần. Hoạt tính luciferase được xác định bằng GloMax Micro khắc Luminometer (Promega). Tỷ lệ trung hòa (%) được tính như sau:
Trung hòaRate (%)
NeutralizationRate(%)
RLUpesudovirus−RLUpesudovirus with serum
= --------------------------------------------------------------- 100%
RLUpesudovirus−RLUblank100%N
Đo độ Cytokines
Huyết thanh của bệnh nhân nhiễm SARS-CoV-2 được xác nhận trong phòng thí nghiệm (nhóm không triệu chứng n = 37 và nhóm triệu chứng n = 37) được thu thập càng sớm càng tốt khi nhập viện. Huyết thanh của những người khỏe mạnh (n = 37) được đưa vào nhóm đối chứng. Nồng độ 48 cytokine và chemokine được đo bằng cách sử dụng Bảng sàng lọc Cytokine của người Bio-Plex (48-Plex số 12007283, Bio-Rad) trên Luminex 200 (Dụng cụ ghép kênh Luminex, Merck Millipore) theo hướng dẫn của nhà sản xuất. Bảng sàng lọc 48 cytokine bao gồm: yếu tố tăng trưởng nguyên bào sợi (FGF), eotaxin, yếu tố kích thích khuẩn lạc bạch cầu hạt (G-CSF), yếu tố kích thích khuẩn lạc bạch cầu hạt (GM-CSF), interferon-gamma (IFN-) -1 beta (IL-1β), chất đối kháng thụ thể interleukin 1 (IL-1RA), interleukin 1 alpha (IL-1α), interleukin-2 thụ thể-alpha (IL-2Rα), interleukin-3 (IL-3), interleukin-3 (IL-3) -12 p40 (IL-12 (p40)), interleukin-16 (IL-16), interleukin-2 (IL-2), interleukin-4 (IL-4), interleukin-5 (IL-5), interleukin- 6 (IL-6), interleukin-7 (IL-7), interleukin-8 (IL-8), interleukin-9 (IL-9), oncogene-alpha (GRO-α), yếu tố tăng trưởng tế bào gan (GRO-α) HGF), interferon alpha-2 (IFN-α2), yếu tố ức chế bệnh bạch cầu (LIF), protein monocyte-chemotactic 3 (MCP-3), interleukin-10 (IL-10), interleukin-12 p70 (IL-12 (p70) )), interleukin-13 (IL-13), interleukin-15 (IL-15), interleukin-17A (IL-17A), protein gây cảm ứng gamma (IP-10), protein hóa trị đơn bào-1 (MCP-1 ), monokine cảm ứng ed bởi gamma interferon (MIG), yếu tố tăng trưởng thần kinh beta (-NGF), yếu tố tế bào gốc (SCF), yếu tố tăng trưởng tế bào gốc-beta (SCGF-), yếu tố dẫn xuất tế bào stromal 1 (SDF-1α), protein viêm đại thực bào-1 alpha (MIP-1α), protein viêm đại thực bào-1 beta (MIP-1β), yếu tố tăng trưởng có nguồn gốc tiểu cầu-BB (PDGF-BB), được điều chỉnh khi kích hoạt, tế bào T bình thường biểu hiện và được tiết ra (RANTES) ), yếu tố hoại tử khối u alpha (TNF-α), yếu tố tăng trưởng nội mô mạch máu (VEGF), chemokine thu hút tế bào T ở da (CTACK), yếu tố ức chế di chuyển đại thực bào (MIF), ligand gây ra apoptosis liên quan đến TNF interleukin-18 (IL-18), yếu tố kích thích đại thực bào (M-CSF) và yếu tố hoại tử khối u-beta (TNF-).
Phân tích thống kê
Tất cả các đặc điểm liên tục được mô tả là trung vị (IQR) và các đặc điểm phân loại được mô tả dưới dạng số (%). Sự khác biệt đáng kể của các đặc điểm liên tục giữa các nhóm kiểm soát không có triệu chứng và không có triệu chứng và không có triệu chứng và khỏe mạnh được xác định bằng xét nghiệm Mann hè Whitney U. So sánh các đặc điểm phân loại đã được thực hiện với thử nghiệm chính xác của Fisher. Ngưỡng giá trị P 0,05 đối với kháng thể và 0,001 đối với các cytokine chỉ ra ý nghĩa. Phương pháp Kaplan Vi Meier được sử dụng để phân tích thời gian phát tán virus trong các nhóm có triệu chứng và không có triệu chứng. Phân tích thống kê được thực hiện bằng phần mềm R (phiên bản 3.6.0).
Phê duyệt
Nghiên cứu đã được phê duyệt bởi Ủy ban Đạo đức của Đại học Y Trùng Khánh (tham khảo số 2020004). Văn bản đồng ý tham gia vào nghiên cứu này được lấy từ tất cả những người tham gia trưởng thành hoặc người giám hộ thay mặt cho trẻ em tham gia vào nghiên cứu này.
Tóm tắt báo cáo
Thông tin thêm về thiết kế nghiên cứu có sẵn trong Tóm tắt Báo cáo Nghiên cứu Tự nhiên được liên kết với bài viết này.
Dữ liệu
Dữ liệu trong nghiên cứu này được cung cấp trong Bộ dữ liệu bổ sung. Dữ liệu hỗ trợ bổ sung có sẵn từ các tác giả tương ứng theo yêu cầu hợp lý. Tất cả các yêu cầu về dữ liệu và tài liệu thô và phân tích sẽ được xem xét bởi các tác giả tương ứng để xác minh xem yêu cầu có thuộc bất kỳ nghĩa vụ sở hữu trí tuệ hoặc bảo mật nào không. Dữ liệu nguồn được cung cấp với bài báo này.
Theo tạp chí https://www.nature.com/
Tin khác
- Lễ Mit tinh và Chung kết Giải bóng đá cộng đồng 2025
- Đại sứ Nguyễn Hồng Thạch gần gũi và gắn bó với bà con Người Việt như một thành viên
- “Thiên thời, địa lợi, nhân hòa” hội tụ trong hai sự kiện lớn cộng đồng
- Trò chuyện ngắn cùng cô gái trẻ năng động Vũ Thùy Linh
- Người lái đò thời chiến
- Trò chuyện ngắn cùng ông Đỗ Văn Tước
- Trò chuyện cùng “Già làng” Doãn Thanh Tùng
- Trò chuyện cùng Hội viên tiêu biểu Hà Thị Thái
- Khai giảng lớp tiếng Việt năm học 2024-2025 tại Làng Sen, Odessa, Ucraina
- Kiev - Đô thị xanh tuyệt đẹp














